2일 업계에 따르면, 미국 바이오플라이스는 골관절염 치료제 로어시비빈트에 대해 내년 초 미국 식품의약국(FDA)에 품목허가를 신청할 예정이다. 이스라엘 제약사 길메드 역시 아람콜에 대해 내년 FDA 품목허가 신청을 계획 중이다.
삼일제약은 현재 로어시비빈트와 아람콜을 기술도입(L/I)해 국내 독점 판권을 보유 중이다.
|
◇“로어시비빈트, 내년 초 FDA NDA 제출”
로어시비빈트는 상업화 초읽기에 들어간 것으로 파악됐다.
삼일제약은 지난 2021년 미국 바이오스플라이스(Biosplice Therapeutics)로부터 1000만달러(140억원)에 로어시비빈트를 기술도입했다. 계약기간은 계약상 비공개다.
삼일제약 관계자는 “최근 바이오스플라이스와 컨퍼런스콜에서 내년 초 FDA에 로어시비빈트 품목허가(NDA) 제출 예정이라고 전달받았다”며 “바이오스플라이스는 FDA와 논의 과정에서 로어시비빈트가 허가 가능성이 높다고 판단했다”고 밝혔다.
로어시비빈트의 FDA 품목 허가를 높게 보는 이유는 임상 3상에서 근본 치료제로서의 효능을 입증했기 때문이다. 로어시비빈트는 276명을 대상으로 한 3년간 장기 임상시험에서 1차 평가지표인 ‘무릎관절 공간 폭’과 2차 평가지표인 ‘통증 지수’ 모두에서 유효성을 입증했다.
로어시비빈트를 3년간 매년 1회식 총 3회 투여한 시험군의 무릎 관절 내측 공간은 0.06㎜ 감소했다. 반면, 2년간(투약군보다 1년 짧은) 위약 대조군은 0.21㎜ 줄었다. 대조군이 3년간 위약 투약을 지속했다면 무릎 관절 공간이 26㎜ 줄어드는 것으로 나타났다. 경증(2등급) 환자군에선 투약군과 대조군 간 35㎜까지 차이가 나는 것으로 확인됐다.
골관절염이 진행되면 뼈와 뼈 사이의 ‘관절 공간’이 좁아진다. 관절 공간은 연골과 관절액으로 채워져 있다. 이 공간이 좁아지면 뼈끼리 직접 닿아 통증과 마찰이 생길 수 있다.
|
삼일제약은 FDA 신청 직후 식품의약품안전처(안전처)에 품목허가를 신청할 예정이다.
그는 “골관절염 근본 치료제에 대한 글로벌 신약은 존재하지 않는 상황”이라며 “로어시비빈트는 골관절염 표준 치료제로 자리 잡을 가능성이 높다”고 내다봤다. 이어 “로어시비빈트가 해외는 물론 국내 골관절염 치료제 판도를 바꿀 것”이라고 자신했다.
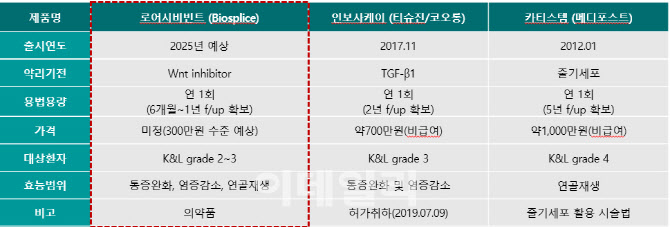
로어시비빈트는 골관절염 2~3기 환자를 대상으로 한 치료제다. 2022년 국내 기준으로 418만 명 중 271만 명(65%)이 2~3등급 환자다.
로어시비빈트 국내 출시 가격은 아직 미정이지만, 경쟁 제품의 절반 이하 또는 1/3 수준인 300만원 내외에서 책정될 전망이다.
삼일제약 관계자는 “로어시비빈트가 시장점유율 10%만 차지한다고 해도 27만명 X 300만원 = 8100억원”이라며 “영업이익률은 20%만 적용해도 1620억원이 나온다”고 추산했다. 이어 “점유율을 절반인 5%라고 가정해도 매출 4000억원에 영업이익 800억원이 나온다”고 덧붙였다.
“아람콜, 상업화 가시권”
아람콜은 기술도입 8년 만에 상업화 가시권에 들어왔다.
삼일제약은 지난 2016년 이스라엘 제약사 ‘갈메드’(Galmed Pharmaceuticals)로부터 ‘비알콜성 지방간염’(NASH) 및 ‘대사이상 지방간염’(MASH) 치료제 ‘아람콜’을 808만달러(113억원)에 기술도입했다.
갈메드는 지난 9월 150명 환자들을 대상으로 한 아람콜의 글로벌 임상 3상 결과를 발표했다. 아람콜 복용 환자에서 간 섬유화 개선이 입증됐다.
아람콜은 간 속 지방은 태워 없애고 탄수화물이 지방으로 전환돼 체내 저장되는 걸 막는다
삼일제약 관계자는 “아람콜은 간에서 지방 대사와 혈당 조절에 관여하는 효소(SCD-1)를 억제해, 간 내 지방을 태우고 혈당을 낮춘다”며 “여기에 에너지 센서(AMPK)를 활성화해 지방 합성을 막고, 탄수화물 분해를 촉진한다”고 기전을 설명했다.
간세포에 과도한 지방이 축적되면 염증이 유발된다. 이 염증은 간세포 손상을 유발하고, 간세포 회복 과정에서 콜라겐이 과도하게 생성돼 간 섬유화가 이뤄진다. 아람콜은 간 섬유화의 원인이 되는 지방간을 없애는 치료제다.
그는 “간세포 손상 → 간 기능 상실 → 간 (조직) 섬유화 순으로 진행된다”며 “간 섬유화가 되면 간 이식 외 치료법이 없다. 아람콜이 세계 최초 간 섬유화 해법으로 등장한 것”이라고 판단했다.
이 같은 성과에 삼일제약이 보유한 아람콜 국내 판권 가치가 치솟았다는 분석이다.
삼일제약 관계자는 “갈메드가 내년 초 아람콜 임상 3상 전체 결과를 발표할 예정”이라며 “곧장 FDA에 NDA 신청에 들어갈 예정이다. 아람콜 FDA 품목허가 후 6개월 정도 시차를 두고 국내 품목허가가 예상된다”고 말했다. 그는 “예전엔 NDA에 1년가량 소요됐다”면서도 “요즘엔 이전보다 빨리 결정이 나는 추세다. 더욱이 아람콜은 FDA 패스트 트랙 지정을 받아 우선심사 적용 대상”이라고 덧붙였다.
삼일제약는 아람콜 국내 출시 후 20년간 독점판매권을 보유 중이다. 아울러 아람콜 베트남 독점 판권에 대한 우선 교섭권도 보유 중이다.
|
아람콜은 글로벌 임상 3상은 12개국(미국, 영국, 호주, 한국, 캐나다, 멕시코, 칠레, 터키, 프랑스, 벨기에, 스페인, 브라질)에 걸쳐 250개 기관에서 2000명 환자를 대상으로 진행 중이다. 국내에선 지난 2019년 식약처 승인을 받아 서울대병원 등 14개 기관에서 아람콜 임상 3/4상이 진행 중이다.
이날 건강보험심사평가원에 따르면 국내 NASH·MASH 환자 수는 40만6000명으로 집계됐다. 올해 3월 FDA 승인을 받은 마드리칼 파마슈티컬스의 NASH 치료제 레스티메티롬의 연간 약가는 1만9000달러(2500만원)으로 알려져있다. 아람콜이 비슷한 약가에 국내 점유율 10%라고 가정하면 ‘2500만원 X 4만명 =1조원’이라는 계산이 나온다.
글로벌 NASH·MASH 치료제 시장은 2021년 37억달러(약 5조원)에서 2026년 58억달러(7조8000억원), 2030년에는 200억달러(27조 원)로 성장할 것으로 예상된다.
삼일제약 관계자는 “기술도입한 아람콜과 로어시비빈트 상업화가 임박했다”며 “두 치료제 모두 FDA 임상 3상에서 확실한 효과를 입증했다. 매출 발생이 임박한 만큼, 파이프라인 가치가 올라갔다”고 진단했다.

.png)











![“심플한데 고급져”…남친룩 정석 변우석 일상 패션[누구템]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/05/PS26050200312t.jpg)
